Retinografie a colori
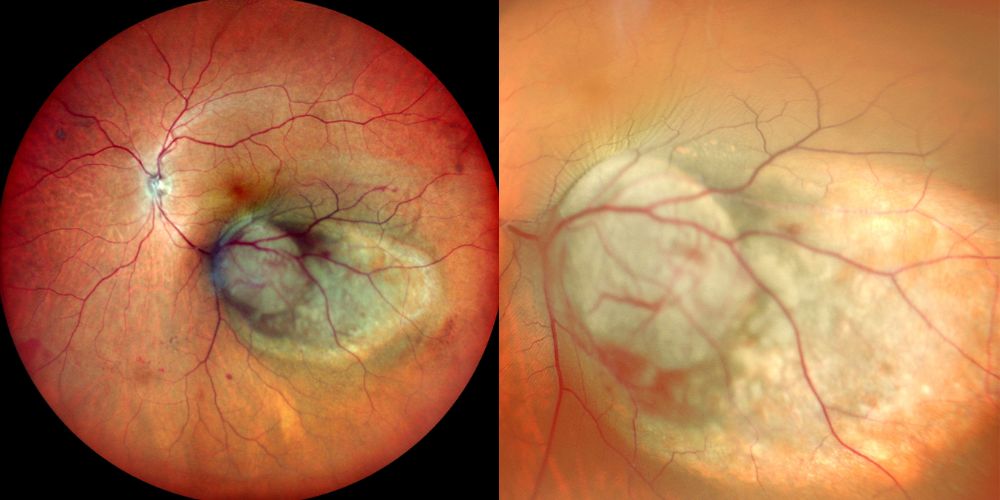
Autofluorescenza
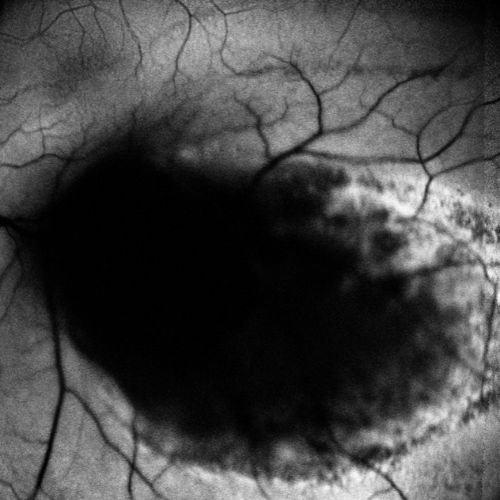
Infrarosso
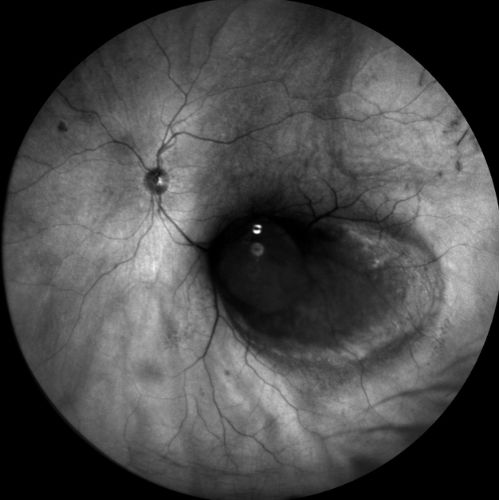
Fluorangiografia
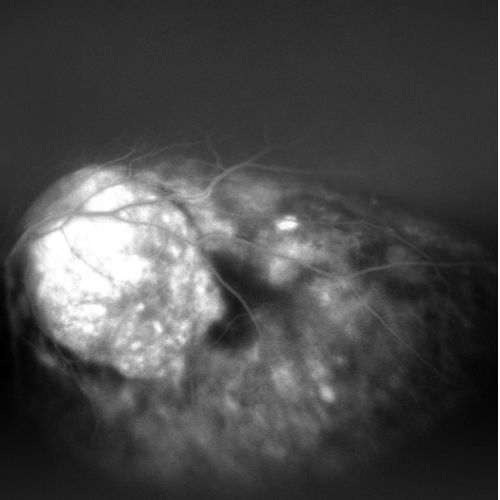
Fluorangiografie
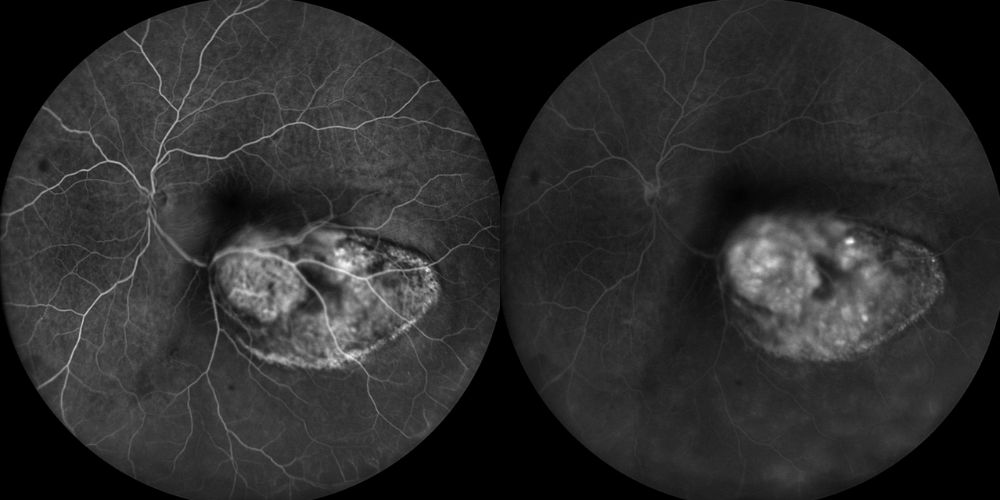
Retromode
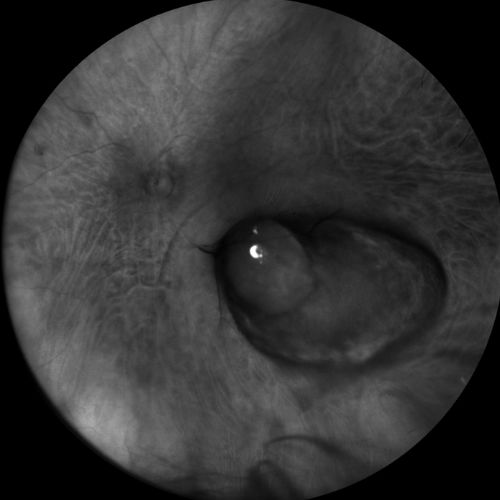
Verde
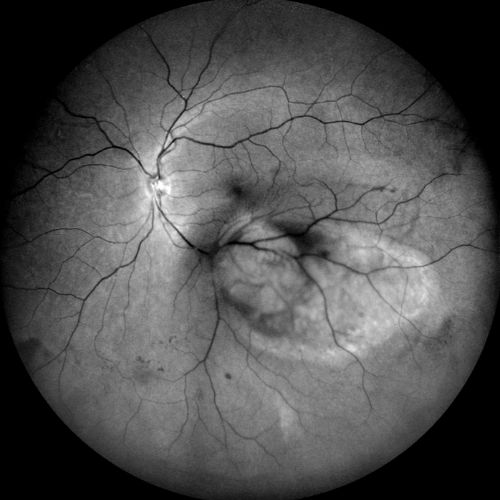
Rosso
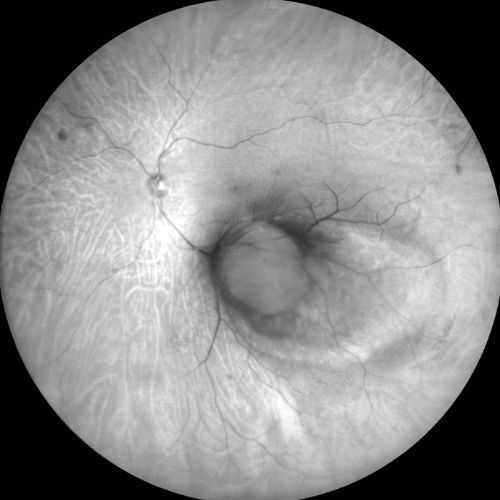
OCT
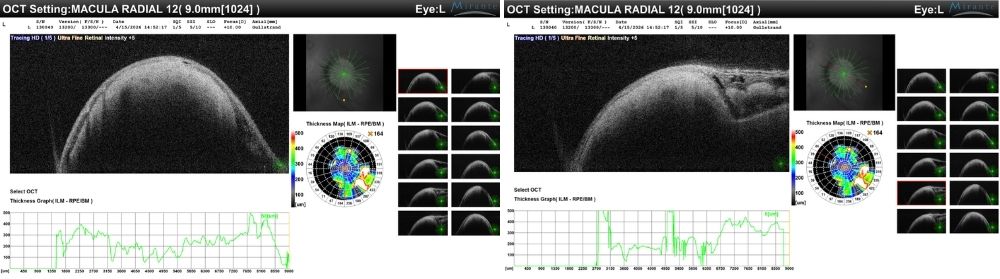
Ecografia A-B scan
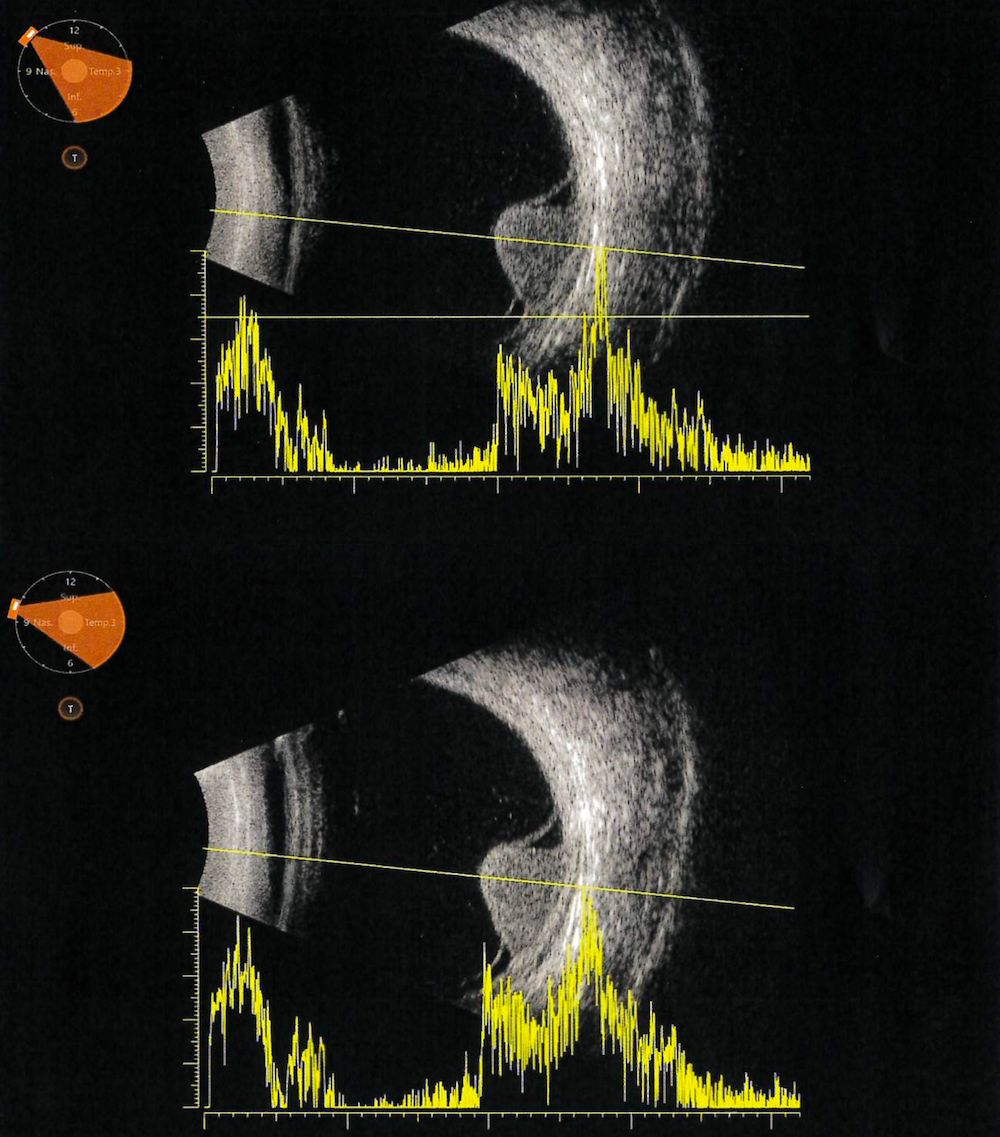
Dalla stadiazione all’enucleazione, dalla brachiterapia alla radioterapia protonica con localizzazione mediante marker di tantalio
Revisione narrativa basata su linee guida, review e studi di riferimento internazionali
1. Inquadramento clinico e stadiazione
Il melanoma della coroide e del corpo ciliare viene oggi inquadrato secondo il sistema AJCC TNM, che integra dimensioni del tumore, coinvolgimento del corpo ciliare, eventuale estensione extrasclerale, interessamento linfonodale e metastasi a distanza. Per il clinico il concetto è semplice: tumori più grandi, anteriori, con coinvolgimento del corpo ciliare o estensione oltre la sclera presentano prognosi peggiore. A questi elementi anatomici si associano oggi fattori istologici e molecolari, come monosomia 3, gain di 8q e perdita di BAP1, che affinano la stima del rischio metastatico.
In un articolo divulgativo-professionale è utile sottolineare che gli stadi iniziali corrispondono a lesioni più piccole e confinate al bulbo, mentre gli stadi avanzati includono masse di maggior volume, con estensione locale o sistemica. Questa impostazione mantiene rigore scientifico ma resta leggibile per il paziente e per il medico non oncologo.
2. Evoluzione del trattamento: dalla chirurgia demolitiva alla conservazione del bulbo
Per molti decenni l’enucleazione è stata il trattamento standard del melanoma coroideale. L’avvento della brachiterapia e poi delle tecniche di radioterapia esterna ad alta precisione ha modificato il paradigma terapeutico: oggi, quando possibile, si tende a ottenere il controllo locale salvando il bulbo. Questo approccio non nasce da una scelta “estetica”, ma da evidenze cliniche robuste secondo cui la conservazione dell’occhio, nei casi appropriati, non compromette la sopravvivenza rispetto alla chirurgia demolitiva.
Il passaggio storico decisivo è stato il Collaborative Ocular Melanoma Study (COMS), che per i melanomi coroideali di medie dimensioni ha mostrato l’assenza di differenze clinicamente o statisticamente significative nella sopravvivenza tra enucleazione e brachiterapia con Iodio-125. Di fatto, la brachiterapia è divenuta il trattamento di riferimento per molti melanomi di piccole e medie dimensioni, aprendo la strada a un approccio sempre più conservativo.
3. Le principali opzioni terapeutiche
| Opzione | Indicazioni principali | Vantaggi | Limiti/complicanze |
|---|---|---|---|
| Enucleazione | Tumori grandi, bulbo doloroso, glaucoma secondario severo, distacco retinico totale non reversibile, invasione del nervo ottico, occhio non conservabile | Radicalità locale, semplicità oncologica, disponibilità istologica completa | Perdita del bulbo e della funzione visiva |
| Brachiterapia episclerale | Piccoli-medi melanomi, soprattutto posteriori e trattabili con corretta copertura dosimetrica | Standard consolidato, sopravvivenza comparabile all’enucleazione nei tumori medi, salvataggio del bulbo | Retinopatia radiante, papillopatia, cataratta, possibile perdita visiva progressiva |
| Radioterapia protonica | Tumori medio-grandi, peripapillari, juxtapapillari, vicini a fovea o nervo ottico, forme irregolari o poco adatte a placca | Alta precisione dosimetrica grazie al Bragg peak, elevato controllo locale, alta probabilità di conservare il bulbo | Complicanze attiniche tardive, calo visivo frequente nei tumori maculari o peripapillari |
| Resezione locale / sclerouvectomia | Casi selezionati, soprattutto alcuni tumori del corpo ciliare o vicini all’equatore | Rimozione della massa con conservazione del bulbo in casi scelti | Tecnica complessa, più complicanze, indicazioni limitate |
| TTT / terapie termiche | Piccolissime lesioni selezionate o uso complementare | Approccio mininvasivo | Non rappresenta il trattamento standard della maggioranza dei melanomi, rischio di recidiva |
In termini pratici, oggi la scelta terapeutica dipende da un equilibrio tra controllo oncologico, anatomia del tumore, probabilità di conservazione del bulbo e aspettativa funzionale. Nei tumori medi posteriori la brachiterapia resta spesso il primo riferimento; nei tumori voluminosi o topograficamente critici, la protonterapia rappresenta una delle opzioni più eleganti e precise.
4. Enucleazione: indicazioni attuali
L’enucleazione non deve essere considerata un fallimento, ma una scelta oncologicamente corretta in casi ben definiti. Resta indicata quando il tumore occupa gran parte delle strutture intraoculari, quando il bulbo è doloroso o complicato da glaucoma neovascolare importante, quando vi è distacco totale non recuperabile, coinvolgimento del nervo ottico o impossibilità tecnica a garantire una terapia conservativa affidabile. Il vantaggio dell’enucleazione è la radicalità locale e l’eliminazione immediata del tumore intraoculare. Il prezzo è la perdita dell’occhio. In alcuni casi complessi o molto avanzati, tuttavia, è la scelta più prudente e più appropriata.
5. Brachiterapia episclerale
La brachiterapia con placca radioattiva è il trattamento più diffuso e meglio consolidato per molti melanomi piccoli e medi. La placca contenente semi radioattivi viene fissata temporaneamente alla sclera in corrispondenza del tumore, così da erogare una dose elevata al bersaglio con relativamente minore irradiazione dei tessuti vicini.
Il COMS ha dimostrato che, nei melanomi medi, la sopravvivenza dopo brachiterapia con Iodio-125 è sovrapponibile a quella osservata dopo enucleazione. Questo risultato ha cambiato in modo definitivo la pratica clinica. Il limite della brachiterapia è geometrico: quando la massa tocca il nervo ottico, è molto ampia alla base o ha una forma sfavorevole, la copertura dosimetrica può risultare meno ideale e la tossicità sulle strutture nobili può aumentare.
6. Radioterapia protonica: razionale e indicazioni
La radioterapia protonica è la forma di radioterapia esterna più collaudata in ottica eye-sparing per il melanoma uveale. Il suo vantaggio fisico deriva dal Bragg peak, cioè dalla capacità dei protoni di depositare la massima dose nel bersaglio con rapida caduta oltre il tumore. Ciò la rende particolarmente utile nei tumori medio-grandi, nei melanomi juxtapapillari o perimaculari, nelle lesioni a contorni irregolari e in generale in tutti i casi in cui la brachiterapia non offra una geometria ottimale.
Le grandi serie e le review moderne riportano per la protonterapia tassi di controllo locale a 5 anni generalmente superiori al 90%, spesso compresi tra 93,9% e 96,5%, con conservazione del bulbo in un’ampia percentuale di casi. Il limite principale non è il controllo del tumore, ma la funzione visiva a lungo termine: se la massa è vicina a fovea o nervo ottico, la probabilità di importante riduzione visiva rimane elevata nonostante l’eccellente controllo locale.
7. Tecnica chirurgico-radioterapica con marker di tantalio: descrizione dettagliata
7.1 Studio preoperatorio
Prima della protonterapia il paziente viene studiato con esame del fundus, retinografia, ecografia, biometria oculare e misurazione della lunghezza assiale. Questi dati sono indispensabili per costruire un modello tridimensionale dell’occhio e del tumore, necessario alla pianificazione dosimetrica.
7.2 Applicazione dei marker di tantalio
Quando il melanoma interessa coroide e/o corpo ciliare, si esegue un intervento chirurgico di localizzazione con applicazione di 3–5 marker episclerali di tantalio in prossimità dei margini tumorali proiettati sulla sclera. Il tantalio è radiopaco: questo consente di renderlo chiaramente visibile durante pianificazione e verifica del trattamento. La funzione dei marker non è terapeutica, ma topografica e geometrica.
Dal punto di vista tecnico, la procedura prevede peritomia congiuntivale, ampia esposizione sclerale, eventuale isolamento o disinserzione temporanea di uno o più muscoli retti quando necessario, e successiva fissazione sclerale dei marker nella posizione pianificata. È fondamentale registrare con precisione i rapporti marker-limbus e i riferimenti anatomici intraoperatori, perché questi dati entrano direttamente nel modello di pianificazione. L’American Academy of Ophthalmology descrive fra i passaggi chiave la conjunctival peritomy, la scleral fixation e l’optimal marker positioning.
7.3 Pianificazione del trattamento
Dopo il posizionamento dei marker, il centro protonico integra nel piano terapeutico biometria, ecografia, fotografie del fundus, posizione dei marker e imaging radiologico di verifica. Su questa base viene creato un modello 3D dell’occhio che definisce il rapporto spaziale tra tumore, marker, cristallino, macula e nervo ottico. In molti protocolli al volume tumorale lordo viene aggiunto un margine per tenere conto di estensione microscopica e incertezze di setup.
Un punto tecnico di grande importanza è la misura della distanza tra margine tumorale e marker di tantalio. La letteratura più recente suggerisce che l’ecografia migliori questa misura rispetto alla sola transilluminazione intraoperatoria. In uno studio pubblicato su Eye, l’integrazione dell’ecografia nel planning ha migliorato il controllo locale a 5 anni rispetto alla transilluminazione da sola, confermando quanto l’accuratezza della localizzazione influenzi il risultato oncologico.
7.4 Erogazione dei protoni
Durante il trattamento il paziente viene immobilizzato con dispositivi dedicati, tipicamente maschera personalizzata e, in alcuni protocolli, bite dentale. La posizione del capo deve essere estremamente riproducibile. L’occhio viene orientato con un target di fissazione visiva, così da presentare il tumore al fascio con il miglior angolo possibile e limitare la dose alle strutture critiche. I marker di tantalio vengono visualizzati nei controlli di setup quotidiani e rappresentano quindi un riferimento essenziale per l’accuratezza della terapia.
Nelle serie storiche più citate, la protonterapia per melanoma uveale viene somministrata in poche frazioni ad alta dose, spesso quattro sedute consecutive. Il messaggio clinico più importante è che la riuscita del trattamento dipende tanto dalla fisica dei protoni quanto dalla precisione del planning e dalla correttezza della localizzazione chirurgica iniziale.
8. Risultati oncologici e funzionali della protonterapia
Le review recenti riportano che la protonterapia ottiene un eccellente controllo locale, generalmente superiore al 90%, con elevati tassi di conservazione del bulbo. In una review del 2024 sono riportati tassi di local control a 5 anni del 93,9–96,5% e tassi di eye preservation del 71,3–95%. In una serie olandese di pazienti inviati in Svizzera per protonterapia, il controllo locale a 5 anni è stato del 94%, la preservazione del bulbo dell’81% e la sopravvivenza libera da metastasi del 70%.
Sul piano funzionale, tuttavia, il limite resta significativo: molti pazienti sviluppano grave riduzione visiva nel tempo, specialmente quando il tumore è centrale o quando la dose alla macula è inevitabilmente elevata. Questo concetto va spiegato bene al paziente: la protonterapia può salvare l’occhio con alta probabilità, ma non garantisce il mantenimento di una buona visione centrale.
9. Complicanze della radioterapia protonica
Le principali complicanze tardive comprendono maculopatia attinica, retinopatia radiante, papillopatia, cataratta, infiammazione intraoculare, emovitreo e glaucoma neovascolare. La review 2024 su radioterapia esterna nel melanoma uveale riporta nelle grandi serie percentuali rilevanti di maculopatia, cataratta, glaucoma e papillopatia. Il rischio di complicanze aumenta naturalmente quando il tumore è vicino a fovea, papilla, corpo ciliare o quando il volume irradiato è maggiore.
Un capitolo specifico è la toxic tumor syndrome: il tumore irradiato può andare incontro a necrosi ischemico-essudativa, con edema maculare, distacco sieroso persistente, rubeosis iridis e glaucoma neovascolare. Ciò spiega perché il follow-up oncologico-oculistico dopo protonterapia debba essere eseguito in centri esperti.
10. In sintesi: come scegliere
L’enucleazione resta la scelta corretta quando il tumore è troppo avanzato o il bulbo non è ragionevolmente salvabile. La brachiterapia è il riferimento per molti melanomi piccoli-medi. La protonterapia, invece, rappresenta una straordinaria opzione di conservazione del bulbo nei tumori più grandi, più posteriori o più vicini a nervo ottico e macula, a condizione che la pianificazione sia impeccabile e che la localizzazione con marker di tantalio sia eseguita con precisione. Nei centri esperti, la corretta integrazione di chirurgia di localizzazione, imaging ecografico e pianificazione tridimensionale costituisce il cuore del successo terapeutico.
Bibliografia essenziale
- National Cancer Institute. Intraocular (Uveal) Melanoma Treatment (PDQ). https://www.cancer.gov/types/eye/hp/intraocular-melanoma-treatment-pdq
- American Academy of Ophthalmology. Diagnosis and Management of Choroidal Melanoma. https://www.aao.org/eyenet/article/diagnosis-and-management-of-choroidal-melanoma
- EyeWiki. Management of Choroidal Melanoma and Ciliary Body Melanoma. https://eyewiki.org/Management_of_Choroidal_Melanoma_and_Ciliary_Body_Melanoma
- COMS Group. The COMS randomized trial of iodine 125 brachytherapy for choroidal melanoma. https://pubmed.ncbi.nlm.nih.gov/12466159/
- Proton Therapy in Uveal Melanoma. Review. https://pmc.ncbi.nlm.nih.gov/articles/PMC11506608/
- External beam radiotherapy in the management of uveal melanoma. Review 2024. https://link.springer.com/article/10.1007/s11864-024-01212-5
- Ultrasonography and transillumination for uveal melanoma localisation in proton beam treatment planning. https://www.nature.com/articles/s41433-019-0512-1
- Proton beam radiotherapy of uveal melanoma. https://pmc.ncbi.nlm.nih.gov/articles/PMC3770228/
- Clinical Outcomes after International Referral of Uveal Melanoma Patients for Proton Therapy. https://pmc.ncbi.nlm.nih.gov/articles/PMC8699723/
- AAO video. Tantalum Ring Placement for Proton Beam Therapy in Uveal Melanoma. https://www.aao.org/education/1-minute-video/tantalum-ring-placement-proton-beam-therapy-in-uve

