Abstract
Riportiamo il caso di un paziente maschio di 50 anni, trapiantato renale per insufficienza renale terminale secondaria a nefropatia da depositi di IgA, con severa storia trombotica sistemica, che ha sviluppato una retinopatia ischemica proliferante unilaterale (occhio sinistro). L’analisi multimodale (retinografia a colori, fluorangiografia – FAG, e tomografia a coerenza ottica – OCT) ha evidenziato un’area di ischemia retinica settoriale superiore complicata da neovascolarizzazione fibrovascolare attiva (aspetto “a gorgonia”). È degno di nota il riscontro, nel medesimo distretto ischemico, di almeno due shunt/collaterali vascolari, interpretabili come rimodellamento adattativo del letto microvascolare cronico. L’OCT ha confermato l’assenza di edema maculare significativo. Il quadro clinico, inquadrabile come esito post-occlusivo (BRVO-like) o microangiopatia occlusiva ischemica, sottolinea lo stretto legame fisiopatologico tra danno microvascolare sistemico (uremia, ipertensione, stato protrombotico) e patologia retinica. Si discute inoltre la diagnosi differenziale e l’approccio terapeutico (laser focale/scatter), sottolineando l’importanza dello screening oftalmologico tempestivo nei pazienti con nefropatia cronica e trapianto renale.
Introduzione
Il legame fisiopatologico tra insufficienza renale cronica (CKD), trapianto renale e malattia vascolare retinica è ampiamente documentato in letteratura. Rene e retina condividono notevoli similitudini strutturali e funzionali a livello microvascolare; pertanto, il danno endoteliale sistemico indotto dall’uremia, dall’infiammazione cronica e dall’ipertensione arteriosa si manifesta spesso sincronicamente in entrambi gli organi17,18.
Dati epidemiologici su ampie coorti hanno confermato l’elevato rischio vascolare oftalmico nei pazienti nefropatici. Lo studio retrospettivo di Lin et al. su una coorte taiwanese di 85.596 pazienti ha dimostrato che la CKD raddoppia il rischio di sviluppare malattie vascolari retiniche (Hazard Ratio [HR] 2.30) indipendentemente dall’età e dalla presenza di ipertensione o diabete8. Nei pazienti con insufficienza renale terminale (ESRD), il rischio di occlusione venosa retinica (RVO) risulta triplicato (HR 3.21) rispetto ai controlli sani9,11,12. Il trapianto renale (KT) riduce significativamente questo rischio rispetto ai pazienti in emodialisi, dimezzandone l’incidenza, ma mantiene comunque un rischio relativo superiore (HR 1.53) rispetto alla popolazione generale, particolarmente in soggetti over 50 con comorbidità multiple10.
In questo delicato equilibrio sistemico, si inserisce anche la patologia di base del paziente: la nefropatia da deposizione di IgA (IgAN o Malattia di Berger). Sebbene rara, in letteratura sono riportati casi di vasculopatia retinica ischemica secondaria a IgAN, ipotizzando come meccanismo patogenetico la deposizione di immunocomplessi IgA a livello del microcircolo retinico, con conseguente infiammazione, occlusione capillare e rimodellamento ischemico13,14.
Presentazione del Caso Clinico
Paziente di sesso maschile, 50 anni, giunto alla nostra attenzione per un controllo oftalmologico. L’anamnesi patologica remota è complessa ed è dominata da una nefropatia da deposizione di IgA (IgAN), evoluta in insufficienza renale terminale (ESRD) che ha richiesto emodialisi dal 2004 al 2005. Ha ricevuto un primo trapianto renale nel 2007 (fossa iliaca destra). Dopo un periodo di sospensione della terapia immunosoppressiva (2017-2020), ha presentato un grave deterioramento della funzionalità del graft, ritornando in dialisi nel 2020.
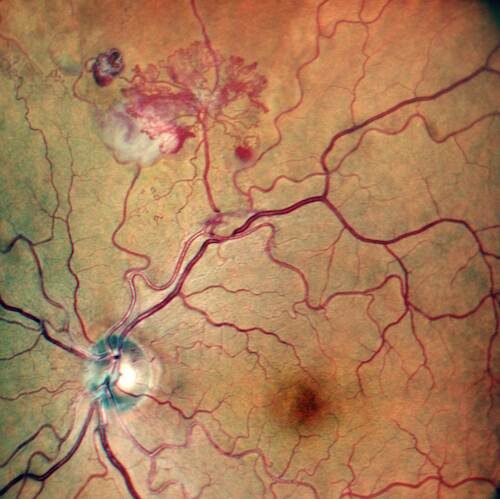
RETINOGRAFIE A COLORI
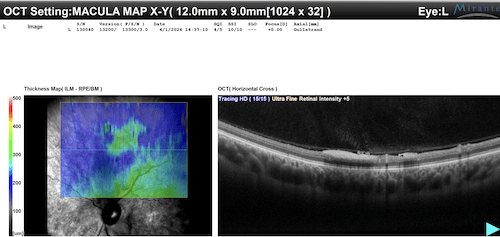
OCT
VERDE
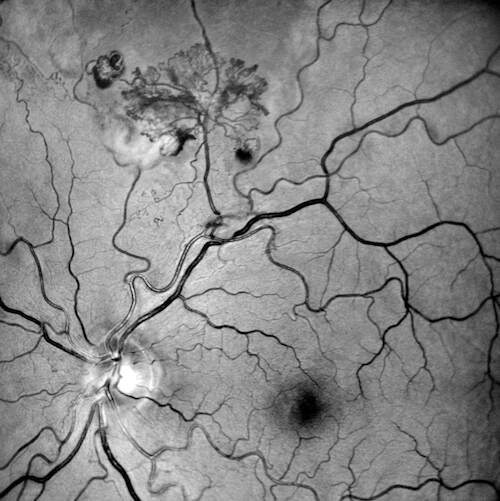
AUTOFLUORESCENZA
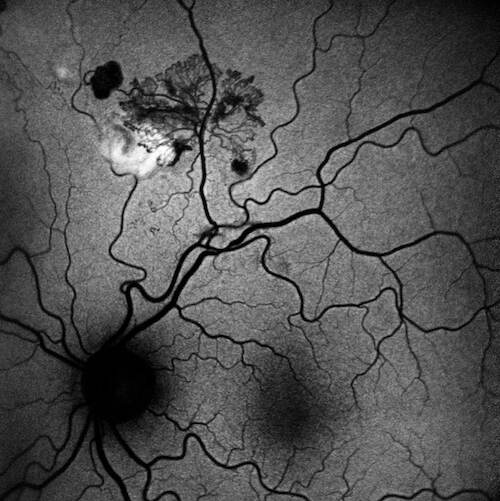
IMAGE ISCHEMIA RETINA WIDE
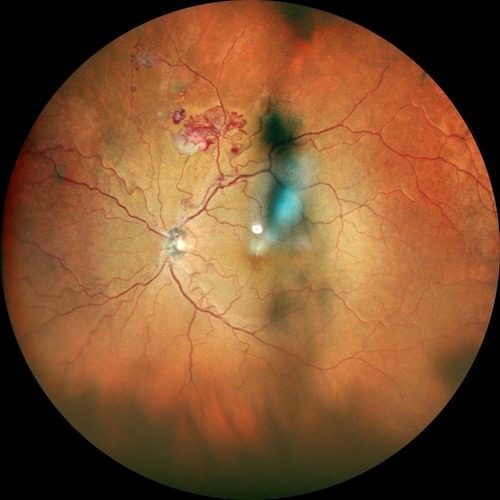
FAG PRECOCI
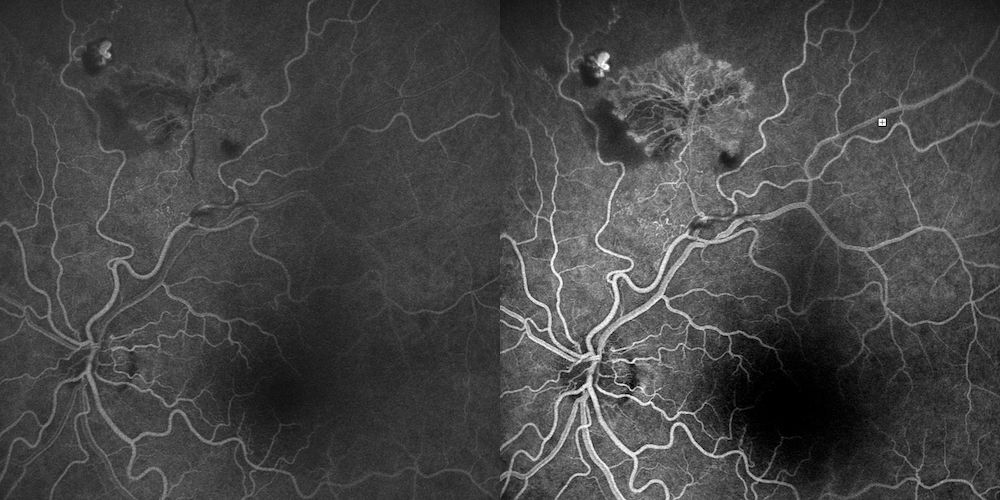
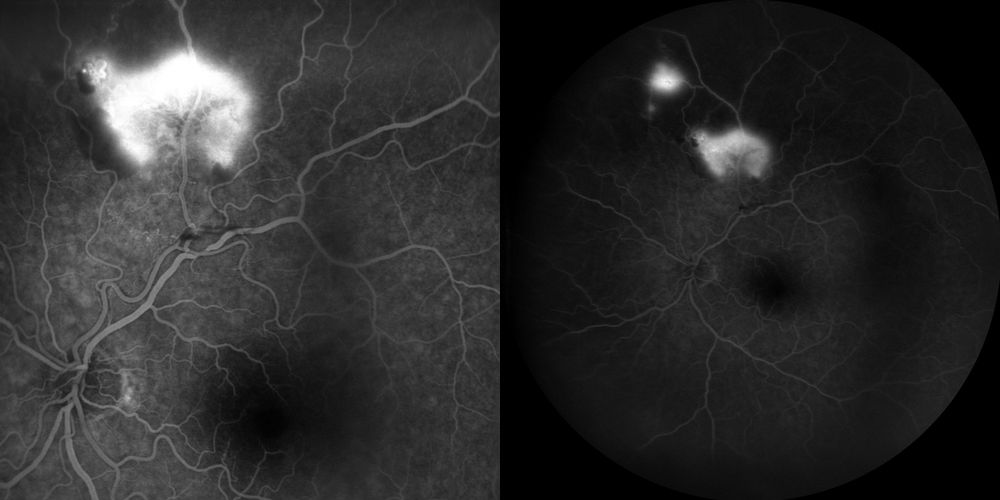
FAG TARDIVE
Nel marzo 2023, il paziente è stato sottoposto a un secondo trapianto renale, complicato da necessità di angioplastica per stenosi dell’arteria iliaca esterna. Il decorso post-operatorio è stato travagliato da: BK-viremia, lieve tossicità da inibitori della calcineurina (documentata da biopsia nel luglio 2023), pielonefrite ascessualizzata (ottobre 2023) e un recente episodio di pielonefrite multifocale da E. coli (maggio 2025).
Significativa è la storia vascolare e trombotica: il paziente ha sofferto di trombosi della vena anticubitale sinistra (2013), trombosi della giugulare interna destra secondaria a CVC (2020) e trombosi dell’arto inferiore destro (agosto 2023). Da settembre 2023 è in terapia anticoagulante cronica con apixaban (2.5 mg bid). È presente ipertensione arteriosa cronica, con episodi storici di crisi severe (es. PAO 180/120 mmHg nel 2020). Non vi è alcuna diagnosi formale di diabete mellito.
Gli esami ematochimici recenti (ricovero maggio 2025) mostrano: creatinina stabile a 1.97 mg/dL (con picchi a 2.5 mg/dL), azotemia 77 mg/dL, glicemia 112 mg/dL, colesterolo totale 205 mg/dL, trigliceridi 92 mg/dL, e una marcata carenza di vitamina D (11.1 ng/mL) con iperuricemia (7.6 mg/dL).
Alla visita oftalmologica, l’occhio destro (OD) si presentava in ordine. L’esame del fundus dell’occhio sinistro (OS) ha invece rivelato un’ampia area ischemica nei settori superiori, complicata da una lesione neovascolare retinica a conformazione “frondiforme/a gorgonia”, associata alla presenza di almeno due shunt/collaterali vascolari nel medesimo distretto superotemporale.
Metodi Diagnostici
Per l’inquadramento morfologico e funzionale della lesione sono state eseguite:
- Retinografia a colori (Fundus Photography): per la documentazione topografica delle lesioni vascolari e ischemiche.
- Fluorangiografia (FAG): acquisizione di sequenze precoci e tardive per valutare la dinamica del flusso vascolare, identificare le aree di non-perfusione capillare e quantificare il grado di attività (leakage) del complesso neovascolare.
- Tomografia a Coerenza Ottica (OCT) maculare: per lo studio strutturale della regione foveale, la valutazione di eventuale edema maculare cistoide e l’identificazione di trazioni vitreomaculari.
Risultati e Analisi delle Immagini Multimodali
Retinografia a Colori
L’esame del fundus dell’OS ha evidenziato, in sede superotemporale, lungo l’arcata vascolare superiore, un complesso vascolare anomalo frondiforme (“a gorgonia”). Tale alterazione è circondata da una componente fibrovascolare di colorito bianco-grigiastro e da piccoli foci emorragici puntiformi o a fiamma adiacenti.
L’analisi morfologica dei vasi permette di distinguere chiaramente la componente arteriolare (calibro minore, riflesso luminoso centrale netto, decorso tendenzialmente rettilineo) dalla componente venosa (calibro maggiore, colorito più scuro, marcata tortuosità).
Reperto chiave: Nel medesimo distretto superiore/superotemporale si apprezzano inoltre almeno due shunt/collaterali vascolari, identificabili come vasi di calibro anomalo con decorso atipico, verosimilmente espressione di rimodellamento del letto vascolare ischemico in risposta all’occlusione cronica. Questo reperto è compatibile con la letteratura sulle occlusioni venose retiniche, che descrive collateral vessels e intraretinal communications come adattamento microvascolare del territorio occluso3,13.
Fluorangiografia (FAG)
L’esame fluorangiografico ha confermato la natura ischemico-proliferativa del quadro:
- Fasi precoci: Rapida iperfluorescenza del complesso vascolare frondiforme.
- Fasi tardive: Marcato e progressivo leakage di colorante (staining e diffusione nei tessuti circostanti), inequivocabile segno di neovascolarizzazione retinica attiva.
- Ischemia: È ben delimitabile una vasta area di alterata/ridotta perfusione capillare retinica nel settore superiore, che funge da substrato ischemico primario per la proliferazione.
- Analisi degli shunt/collaterali: Gli shunt/collaterali vascolari apprezzati alla retinografia si confermano come vasi ad iperfluorescenza tardiva relativamente contenuta rispetto al complesso neovascolare principale, con pattern angiografico compatibile con canali vascolari di remodelling piuttosto che con neovasi attivi con leakage intenso. Questo pattern è in accordo con la letteratura che distingue i collaterali — caratterizzati da iperfluorescenza stabile senza leakage marcato — dai neovasi — caratterizzati da leakage progressivo nelle fasi tardive3.
È essenziale notare l’assenza di staining diffuso della parete vascolare o di segni di perivasculitis (come il fern-like leakage), che rende altamente improbabile l’ipotesi di una vasculite retinica in fase attiva. Allo stesso modo, non si rilevano dilatazioni sacciformi o fusiformi tipiche del macroaneurisma arterioso, escludendolo come lesione patogenetica primaria.
OCT Maculare
Le scansioni OCT a livello del polo posteriore OS documentano un quadro favorevole:
- Profilo foveale e depressione foveale sostanzialmente conservati.
- Assoluta assenza di edema maculare cistoide (CME) o di fluido sottoretinico (SRF).
- In corrispondenza dell’arcata superiore si nota una modesta componente superficiale/preretinica iperriflettente, coerente con il tessuto fibrovascolare osservato oftalmoscopicamente, priva tuttavia di significativa trazione sulla macula.
| Metodica | Reperti Principali | Significato Clinico |
|---|---|---|
| Retinografia | Complesso frondiforme superotemporale con area fibrovascolare bianco-grigia e foci emorragici. Presenza di almeno due shunt/collaterali vascolari. | Neovascolarizzazione fibrovascolare con segni di rimodellamento vascolare cronico (shunt). |
| FAG | Area di non-perfusione superiore. Leakage tardivo marcato dal ciuffo neovascolare. Iperfluorescenza contenuta degli shunt. Assenza di staining vasale diffuso. | Ischemia retinica settoriale con NVE (neovascolarizzazione altrove) attiva. Esclusione di vasculite diffusa e macroaneurisma. |
| OCT | Profilo maculare conservato. Assenza di fluido intra/sottoretinico. Materiale iperriflettente preretinico superiore. | Assenza di complicanze maculari (edema/trazione). Funzione visiva centrale preservata. |
Discussione
Il caso clinico presentato offre uno spunto di riflessione sulle molteplici cause di ischemia retinica in un paziente ad altissima complessità internistica. Il reperto primario è una retinopatia ischemica proliferante settoriale superiore, inquadrabile come esito post-occlusivo venoso (BRVO-like) o microangiopatia occlusiva ischemica.
Meccanismi fisiopatologici sistemici: Il substrato ischemico è la diretta conseguenza di molteplici fattori di rischio sinergici. Il paziente presenta uno stato procoagulante marcato, testimoniato da tre distinti episodi di trombosi venosa profonda (anticubitale, giugulare e arto inferiore) che hanno richiesto l’introduzione di anticoagulanti orali diretti (apixaban). A ciò si aggiunge la disfunzione endoteliale cronica indotta da anni di uremia (ESRD) e l’ipertensione arteriosa severa, i cui picchi documentati (es. 180/120 mmHg) causano alterazioni emodinamiche brusche, inducendo vasospasmo, arteriosclerosi e occlusione microvascolare4-7,15,16.
Il ruolo della nefropatia da IgA: Sebbene il quadro sia fortemente compatibile con una sequela microtrombotica post-occlusiva, non si può escludere un contributo patogenetico della malattia autoimmune di base. El Matri et al. (2021) hanno descritto un caso di vasculopatia retinica ischemica bilaterale associata alla malattia di Berger. Il meccanismo ipotizzato è la deposizione di immunocomplessi IgA circolanti all’interno dei capillari retinici (analogamente al mesangio renale), innescando infiammazione locale, aggregazione piastrinica e trombosi secondaria13.
Significato degli shunt/collaterali vascolari: La presenza di almeno due shunt/collaterali vascolari nel territorio ischemico superiore rappresenta una risposta di rimodellamento adattativo del microcircolo retinico, analoga a quanto descritto nella letteratura sulle occlusioni venose retiniche di branca (BRVO). In questi quadri, la vascolarizzazione collaterale si sviluppa come meccanismo di bypass del territorio occluso, con trasformazione di capillari pre-esistenti in canali di drenaggio alternativo. Romano et al. (2023) descrivono la vascular collateralization come “trasformazione di uno o più capillari in vene, che coinvolge il territorio occluso e le aree vicine”3. Nel caso specifico della vasculopatia retinica ischemica da IgA nephropathy, El Matri et al. hanno evidenziato con SS-OCT-A la presenza di shunt vessels e telangiectatic capillaries ai bordi delle aree ischemiche, un reperto morfologicamente e concettualmente molto simile a quanto osservato nel nostro paziente13.
Diagnosi Differenziale: L’ipotesi principale è quella di una pregressa occlusione venosa di branca ischemica (BRVO) con neovascolarizzazione secondaria, fortemente supportata dai fattori di rischio sistemici. Altre opzioni, come la retinopatia diabetica proliferante, sono escluse dall’anamnesi e dai valori glicemici normali. Il macroaneurisma arterioso è poco probabile per l’assenza di classiche dilatazioni sacciformi alla FAG, mentre una vasculite retinica primaria è smentita dalla mancanza di staining parietale vascolare diffuso all’esame angiografico.
Terapia e Follow-up Consigliati
Sulla base delle attuali linee guida EURETINA1 e del Royal College of Ophthalmologists2 per la gestione dell’ischemia e della neovascolarizzazione post-occlusiva:
Trattamento primario: Fotocoagulazione laser settoriale scatter (PRP settoriale) mirata sull’area ischemica superiore e ai margini del complesso neovascolare. L’obiettivo è distruggere il tessuto retinico ischemico per abbattere la produzione di VEGF e favorire la regressione dei neovasi frondiformi, riducendo il rischio di emorragia vitreale.
Terapia farmacologica di supporto: Le iniezioni intravitreali di farmaci anti-VEGF non sono l’indicazione primaria in assenza di edema maculare, ma possono essere prese in considerazione come terapia adiuvante (spesso associata al laser) qualora si registrasse un leakage molto aggressivo, comparsa di emorragie preretiniche/vitreali, o necessità di indurre una rapida regressione del tessuto fibrovascolare prima di un eventuale approccio chirurgico19,20.
Follow-up Oculistico: Controllo clinico stretto a 4-6 settimane dal trattamento laser per valutare la reazione tissutale. Successivamente, rivalutazioni a 2-3 mesi con fundus oculi, retinografia e OCT. La ripetizione della FAG è indicata qualora vi siano dubbi sulla persistenza di leakage attivo.
Gestione Sistemica: Fondamentale la collaborazione multidisciplinare. È raccomandata una valutazione nefrologica e internistica per l’ottimizzazione del controllo pressorio, il monitoraggio della funzionalità del trapianto e la rigorosa gestione della terapia anticoagulante (apixaban) vista la severa diatesi trombotica del paziente.
Conclusioni Cliniche
Formula diagnostica: Retinopatia ischemica proliferante settoriale superiore OS con neovascolarizzazione fibrovascolare attiva, almeno due shunt/collaterali vascolari e ischemia retinica settoriale superiore, in paziente trapiantato renale ad alto rischio vasculoprotrombotico. Il quadro è verosimilmente post-occlusivo (BRVO-like) o espressione di microangiopatia occlusiva ischemica in contesto nefrovascolare complesso. Assenti segni convincenti di vasculite retinica attiva e macroaneurisma come lesione dominante. OCT maculare senza edema né trazione significativa.
Questo caso evidenzia la cruciale necessità di inserire lo screening oftalmologico strumentale nei protocolli di follow-up per pazienti con Chronic Kidney Disease (CKD) ed End-Stage Renal Disease (ESRD), specialmente in presenza di pregressi eventi trombotici, al fine di intercettare precocemente il danno microvascolare prima dell’insorgenza di gravi complicanze visive.
Bibliografia
- Schmidt-Erfurth U, Garcia-Arumi J, Gerendas BS, et al. Guidelines for the management of retinal vein occlusion by the European Society of Retina Specialists (EURETINA). Ophthalmologica. 2019;242(3):123-162.
- Nicholson L, Talks SJ, Amoaku W, et al. Retinal vein occlusion (RVO) guideline: executive summary. Eye. 2022;36:909-912.
- Romano F, Lamanna F, Gabrielle PH, et al. Update on retinal vein occlusion. Asia-Pac J Ophthalmol. 2023;12(2):196-210.
- Grunwald JE, Alexander J, Ying GS, et al. Retinopathy and chronic kidney disease in the Chronic Renal Insufficiency Cohort (CRIC) study. Arch Ophthalmol. 2012;130(9):1136-1144.
- Grunwald JE, Pistilli M, Ying GS, et al. Association between progression of retinopathy and concurrent progression of kidney disease: findings from the chronic renal insufficiency cohort (CRIC) study. JAMA Ophthalmol. 2019;137(7):767-774.
- Grunwald JE, Pistilli M, Ying GS, et al. Retinopathy and the risk of cardiovascular disease in patients with chronic kidney disease (from the Chronic Renal Insufficiency Cohort study). Am J Cardiol. 2015;116(11):1710-1715.
- Grunwald JE, Pistilli M, Ying GS, et al. Progression of retinopathy and incidence of cardiovascular disease: findings from the Chronic Renal Insufficiency Cohort Study. Br J Ophthalmol. 2021;105(2):246-251.
- Lin JW, et al. Chronic kidney disease as a potential risk factor for retinal vascular disease: A 13-year nationwide cohort study in Taiwan. Medicine (Baltimore). 2021;100(15):e25475.
- Lee KS, Nam KH, Kim DW, et al. Risk of retinal vein occlusion in patients with end-stage renal disease: a 12-year, retrospective, nationwide cohort study in South Korea. Invest Ophthalmol Vis Sci. 2018;59(1):39-46.
- Lee J, Choe HR, Park SH, et al. Impact of kidney transplantation on the risk of retinal vein occlusion in end-stage renal disease. Sci Rep. 2021;11(1):10850.
- Chen SN, Yang TC, Lin JT, Lian IB. End stage renal disease as a potential risk factor for retinal vein occlusion. Medicine (Baltimore). 2015;94(46):e2060.
- Chang YS, Weng SF, Chang C, et al. Risk of retinal vein occlusion following end-stage renal disease: A retrospective, nationwide, matched cohort study. Medicine (Baltimore). 2016;95(16):e3425.
- El Matri K, Amoroso F, Zambrowski O, Miere A, Souied EH. Multimodal imaging of bilateral ischemic retinal vasculopathy associated with Berger’s IgA nephropathy: case report. BMC Ophthalmol. 2021;21(1):424.
- Sakuma A, Ogata T, Wakuta M, Orita T. Retinal pigment epithelial detachment associated with Immunoglobulin A nephropathy: a case report. Case Rep Ophthalmol. 2022;13(3):834-839.
- Hsieh TC, Chou CL, Chen JS, et al. Risk of mortality and of atherosclerotic events among patients who underwent hemodialysis and subsequently developed retinal vascular occlusion: a Taiwanese retrospective cohort study. JAMA Ophthalmol. 2016;134(6):672-679.
- Stem MS, Talwar N, Comer GM, Stein JD. A longitudinal analysis of risk factors associated with central retinal vein occlusion. Ophthalmology. 2013;120(2):362-370.
- Yip W, Ong PG, Teo BW, et al. Retinal vascular imaging markers and incident chronic kidney disease: a prospective cohort study. Sci Rep. 2017;7(1):9374.
- Maguire M, et al. Assessment of retinal microangiopathy in chronic kidney disease patients. Med Arch. 2020;74(3):191-195.
- Macaron MM, Al Sabbakh N, Shami MZ, et al. Anti-VEGF injections vs. Panretinal photocoagulation laser therapy for proliferative diabetic retinopathy: A systematic review and Meta-Analysis. Ophthalmol Retina. 2025.
- Chatziralli IP, Jaulim A, Peponis VG, et al. Branch retinal vein occlusion: treatment modalities: an update of the literature. Semin Ophthalmol. 2014;29(2):85-107.

