SOMMARIO
Cosa è la malattia di Best
Caso n.1
Caso n.2
Cosa è la malattia di Best
La Distrofia Vitelliforme Maculare di Best (BVMD), conosciuta anche come malattia di Best, rappresenta una delle più affascinanti e complesse sfide dell’oculistica contemporanea. Questa condizione genetica, che colpisce la vista centrale, porta con sé una serie di sintomi e complicazioni che richiedono un’attenzione costante e una gestione mirata.
Una Malattia Rara con Impatto Profondo
La BVMD, sebbene rara, è una malattia che può influenzare significativamente la qualità della vita dei pazienti. La sua prevalenza è stimata tra 1/5.000 e 1/67.0000, con una leggera predisposizione verso il sesso maschile. I sintomi esordiscono generalmente durante l’infanzia o l’adolescenza, con una visione normale alla nascita che, nel corso del tempo, subisce un progressivo deterioramento.
Una Progressione complicata
La BVMD passa attraverso diversi stadi, ognuno dei quali porta con sé sintomi e caratteristiche peculiari. Dalla fase asintomatica iniziale, si passa alla formazione della caratteristica lesione “a tuorlo d’uovo” nella macula, seguita dalla comparsa di una sostanza vitellina che può portare alla formazione di cicatrici e al conseguente decadimento dell’acuità visiva centrale. La malattia può essere complicata dalla comparsa di una membrana neovascolare coroideale, che può peggiorare ulteriormente la prognosi visiva.
Ha una origine genetica
La BVMD è caratterizzata da mutazioni nel gene BEST1, localizzato sul cromosoma 11q12, che porta alla produzione anomala di una proteina chiamata bestrofina-1. Questa anomalia comporta un accumulo di lipofuscina, una sostanza che danneggia l’epitelio pigmentato retinico e contribuisce alla disfunzione della visione centrale.
Fondamentale una diagnosi completa e precisa
La diagnosi della BVMD richiede una valutazione clinica accurata, che può includere l’anamnesi familiare, l’esame del fondo dell’occhio e l’utilizzo di tecniche diagnostiche avanzate come la floroangiografia e la OCT. La conferma della diagnosi avviene attraverso lo screening genetico.
Trattamento
Il trattamento della BVMD si basa principalmente sulla gestione dei sintomi e sulla prevenzione delle complicanze. Gli interventi terapeutici possono includere l’utilizzo di ausili per ipovedenti, l’evitare il fumo per ridurre il rischio di complicazioni vascolari e l’impiego di terapie come la fotodinamica o gli agenti anti-VEGF per il trattamento della membrana neovascolare coroideale.
La prognosi è variabile
La prognosi della BVMD è estremamente variabile e dipende da una serie di fattori, inclusa la gravità della condizione e la risposta individuale alla terapia. Mentre alcuni pazienti possono mantenere una buona visione per tutta la vita, altri possono sviluppare complicanze gravi che influenzano significativamente la loro capacità visiva.
In conclusione, la Distrofia Vitelliforme Maculare di Best rappresenta una sfida clinica e scientifica complessa, che richiede un approccio multidisciplinare e una gestione personalizzata per garantire il miglior risultato possibile per i pazienti affetti.
Caso n.1
Questo paziente è giunto alla nostra osservazione 4 anni fa per una Distrofia vitelliforme maculare o malattia di Best. All’inizio è visibile in occhio destro la macchia gialla stratificata in retinografia, nella OCT la macchia risulta iperdensa nella parte inferiore e ipodensa nella superiore.
Alla fluorangiografia risulta ipofluorescente la parte giallastra perché maschera la retina sottostante, mentre è iperfluorescente nella parte superiore per un accumulo del colorante.
Si assiste poi nell’occhio destro ad un riassorbimento del materiale giallastro e al suo posto si atrofizza la retina, come risulta ben evidente all’OCT.
Nell’occhio sinistro, che all’inizio appare quasi normale con poco accumulo di materiale sottoretinico, si assiste negli anni ad un progressivo accumulo di materiale.

Dettaglio delle immagini del paziente seguito da 4 anni:
2020

2022

2024
Caso n.2
La malattia di Best, o distrofia maculare vitelliforme, è una rara patologia genetica che colpisce la macula, l’area centrale della retina responsabile della visione nitida e dettagliata. Tipicamente si manifesta nell’infanzia o nell’adolescenza, ma la sua progressione e la gravità dei sintomi possono variare notevolmente tra i pazienti e, come vedremo in questo caso, anche tra i due occhi dello stesso individuo. In questo articolo, presentiamo un caso clinico emblematico di un paziente di 42 anni che illustra la classica presentazione asimmetrica della malattia, con un occhio che conserva una funzione visiva perfetta nonostante le alterazioni strutturali e l’altro che mostra un calo visivo significativo.
Il Caso Clinico
Un uomo di 42 anni, con diagnosi nota di malattia di Best, si è presentato alla nostra osservazione per un controllo di routine. Il paziente non riferiva nuovi sintomi in occhio destro (OD), mentre lamentava una visione ridotta e stabile da tempo in occhio sinistro (OS).
L’esame dell’acuità visiva ha rivelato un quadro sorprendentemente asimmetrico:
• Occhio Destro (OD): Acuità visiva corretta di 10/10. Il paziente è completamente asintomatico.
• Occhio Sinistro (OS): Acuità visiva corretta di 4/10. Il paziente percepisce una macchia (scotoma) che disturba la visione centrale.
L’esame del fondo oculare e la diagnostica per immagini hanno permesso di correlare perfettamente il quadro clinico con le alterazioni retiniche.
Analisi dell’Occhio Destro (OD)
Nonostante un acuità visiva perfetta, l’occhio destro mostrava chiare alterazioni patologiche.
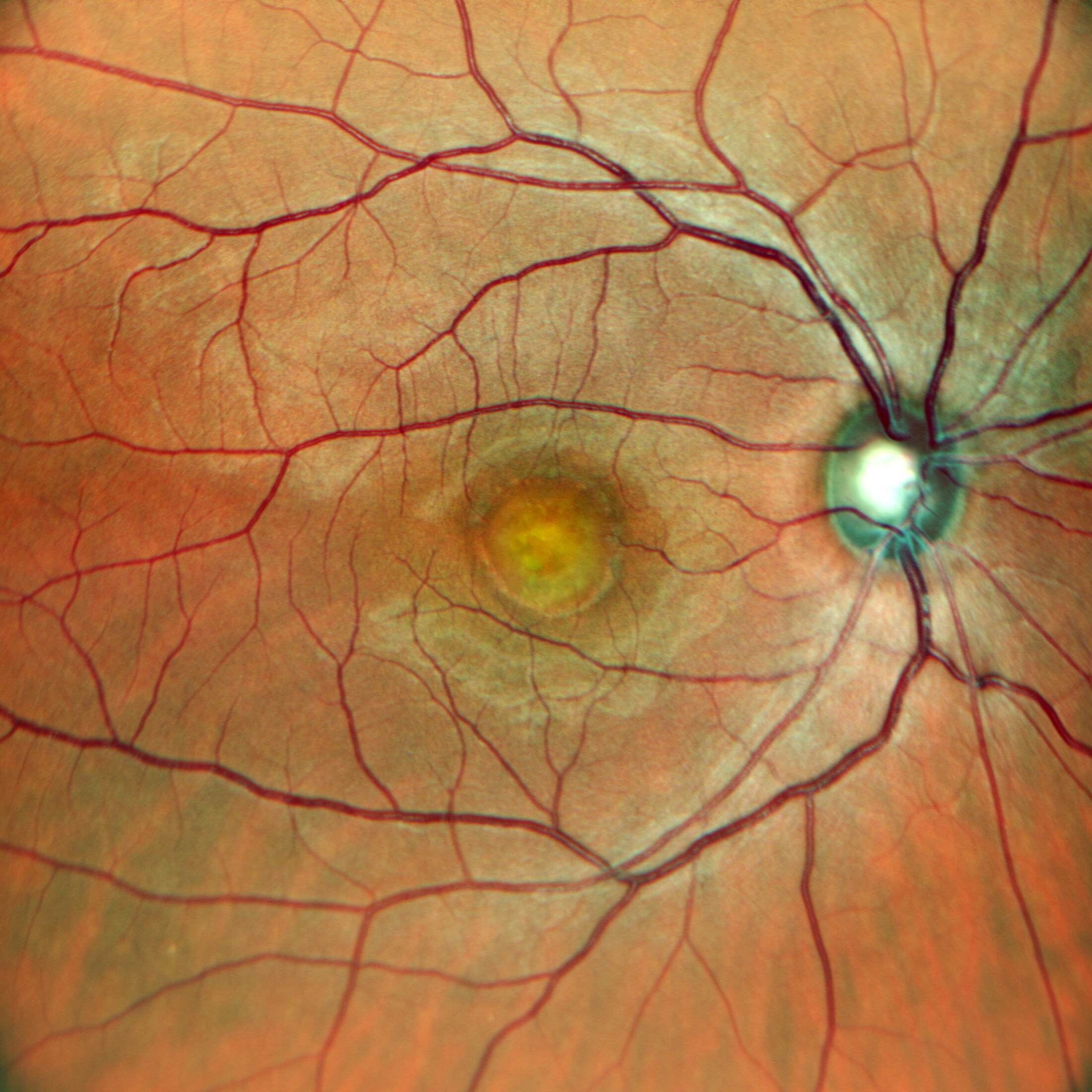
Retinografia (Figura 1): L’esame del fondo oculare ha rivelato la presenza di una classica lesione vitelliforme sub-foveale, una lesione giallastra, rotondeggiante e ben circoscritta, simile a un tuorlo d’uovo (da cui il nome “vitelliforme”).
Figura 1: Retinografia a colori dell’occhio destro (RETINOOD.bmp). Si nota la lesione vitelliforme giallastra al centro della macula.
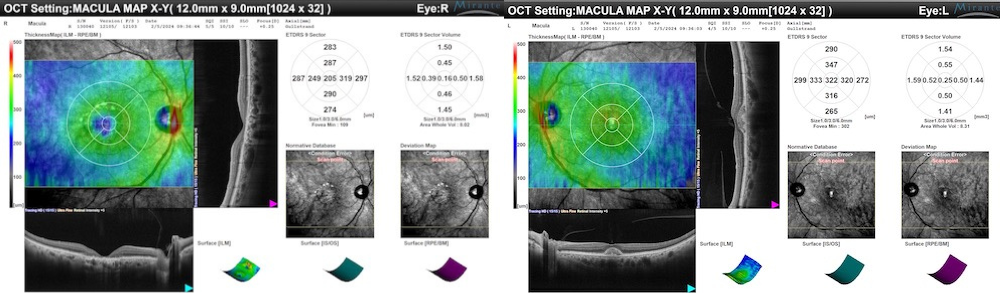
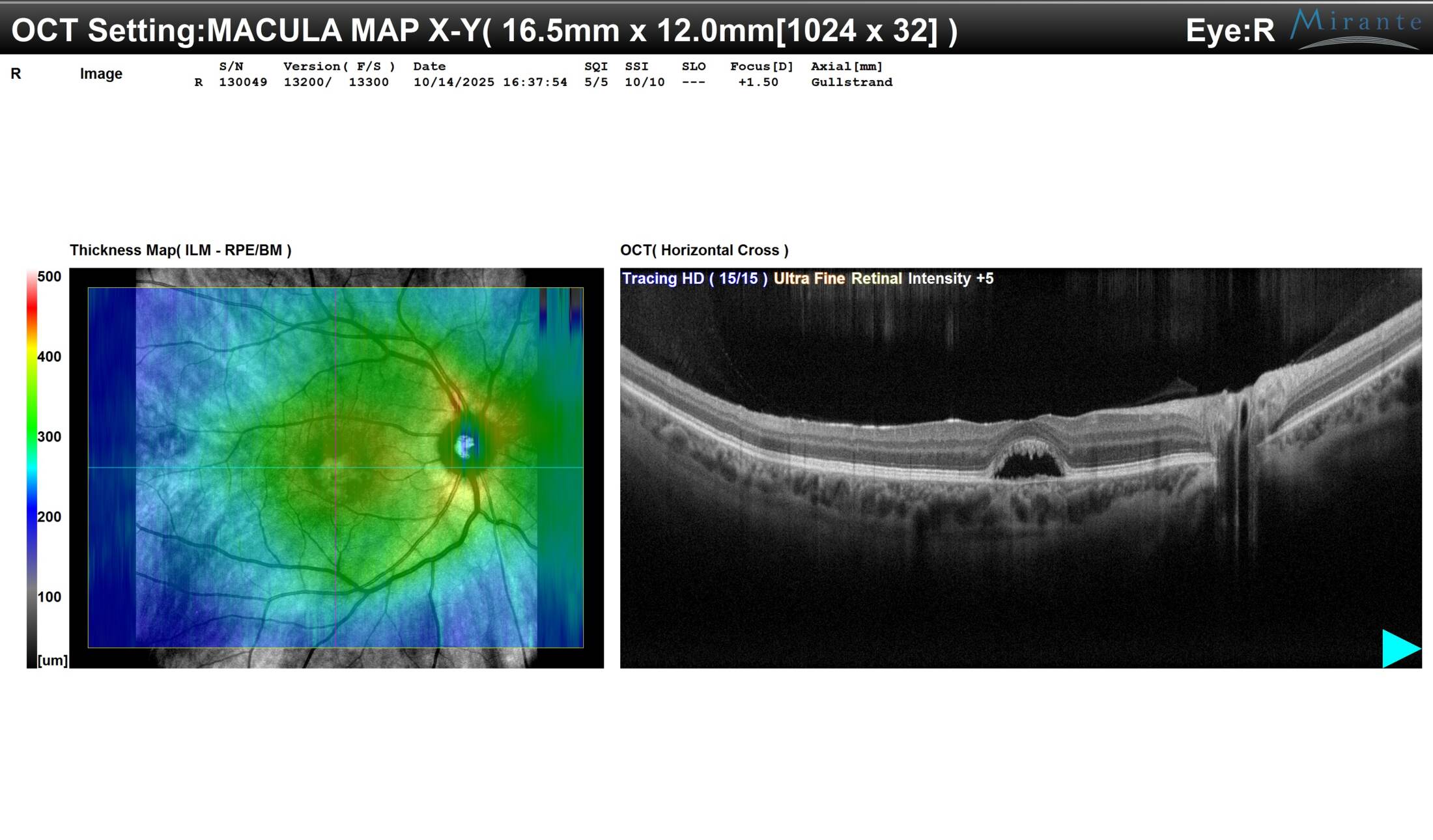
Tomografia a Coerenza Ottica – OCT (Figura 2): L’OCT, un esame che fornisce una scansione ad alta risoluzione degli strati retinici, ha confermato la presenza di un distacco sieroso del neuroepitelio. Il materiale vitelliforme si accumula sotto la retina sensoriale, sollevandola. È importante notare come, nonostante questo sollevamento, gli strati retinici esterni e i fotorecettori appaiano strutturalmente ben conservati, il che spiega l’eccellente acuità visiva.
Figura 2: OCT maculare dell’occhio destro (OCTOD.bmp). La scansione mostra chiaramente il materiale iper-riflettente (giallo) che causa il distacco sieroso della retina neurosensoriale.
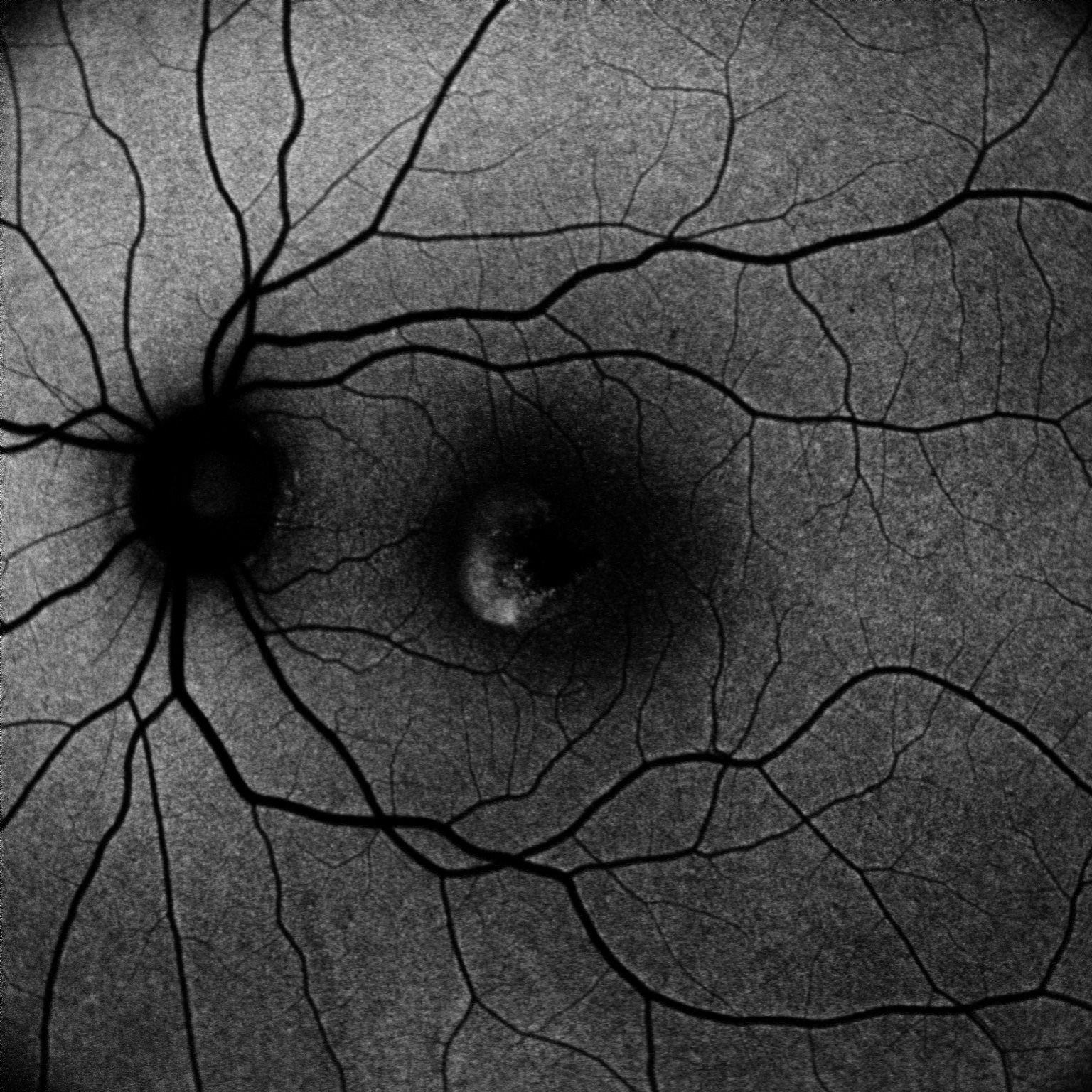
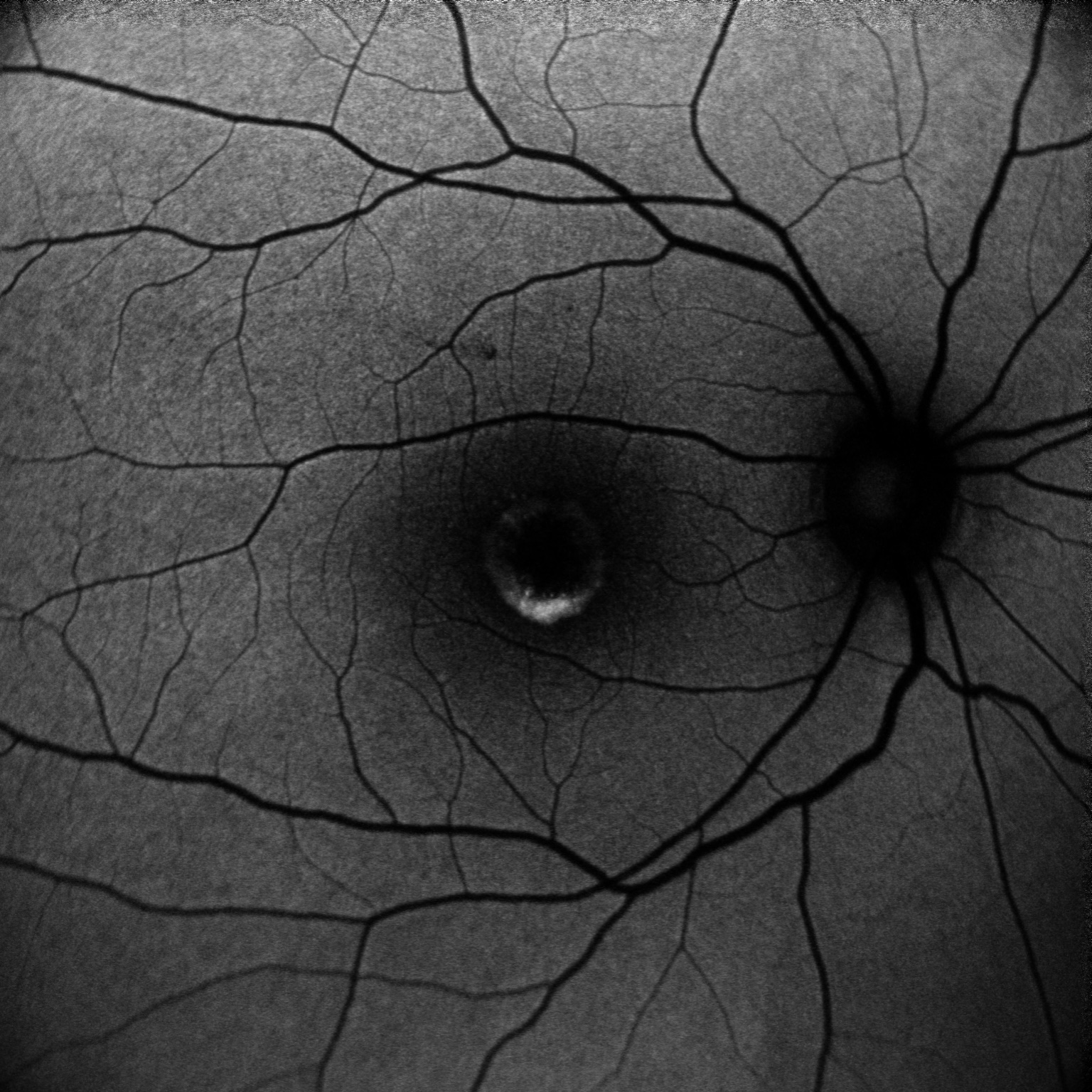
Autofluorescenza (Figura 3): L’esame dell’autofluorescenza, che valuta la salute dell’epitelio pigmentato retinico (EPR), ha mostrato una netta iper-autofluorescenza in corrispondenza della lesione, tipica dell’accumulo di lipofuscina attiva nella fase vitelliforme.
Figura 3: Autofluorescenza dell’occhio destro (AUTOFOD.bmp). L’area della lesione appare intensamente bianca (iper-autofluorescente), indicando stress metabolico dell’EPR ma ancora vitalità.
Analisi dell’Occhio Sinistro (OS)
L’occhio sinistro rappresenta uno stadio più avanzato della malattia, spiegando la ridotta acuità visiva.
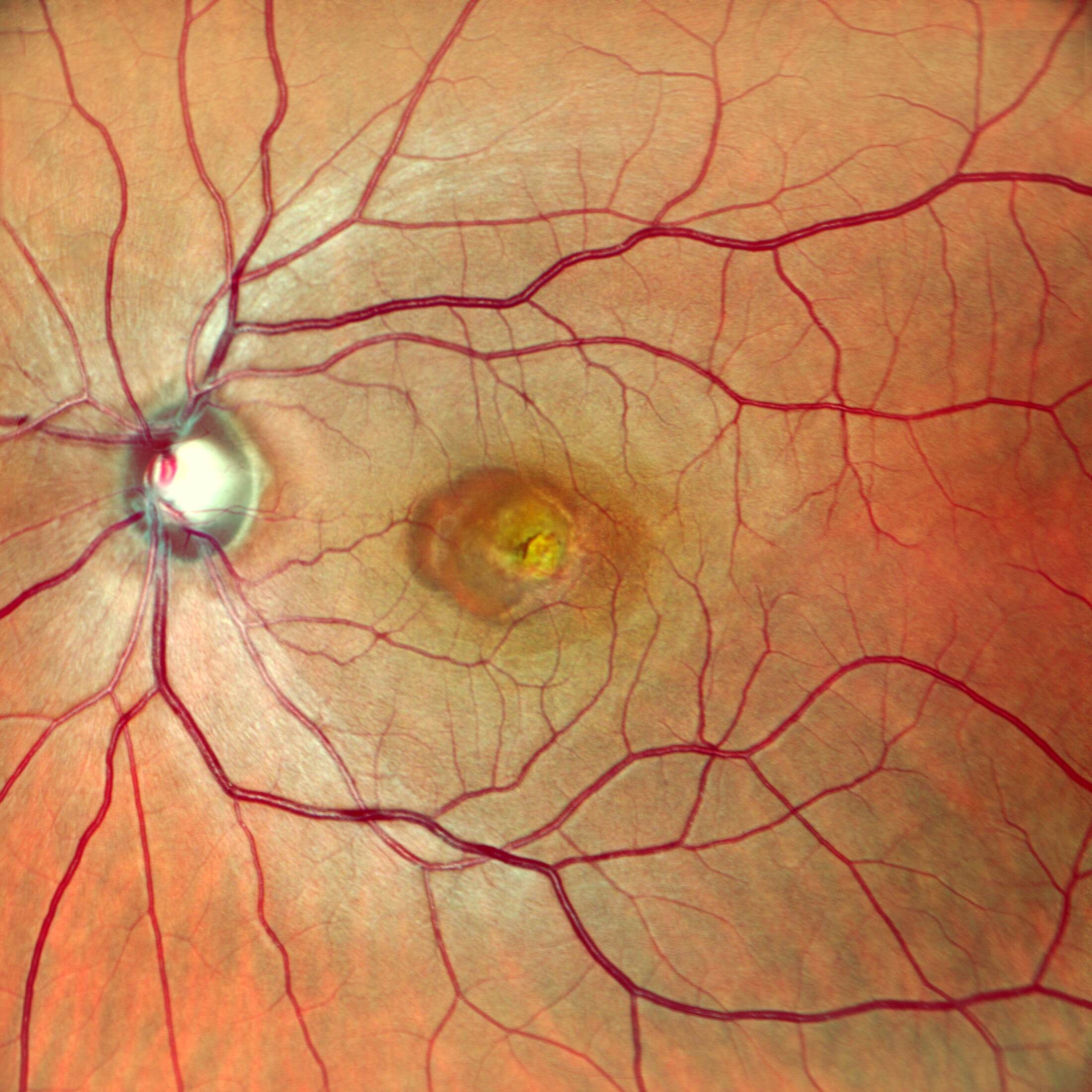
Retinografia (Figura 4): Anche qui è presente una lesione vitelliforme, ma il suo aspetto è meno omogeneo, suggerendo un’evoluzione verso la fase atrofica.
Figura 4: Retinografia a colori dell’occhio sinistro (RETINOOS.bmp). La lesione centrale appare meno compatta rispetto all’occhio destro.
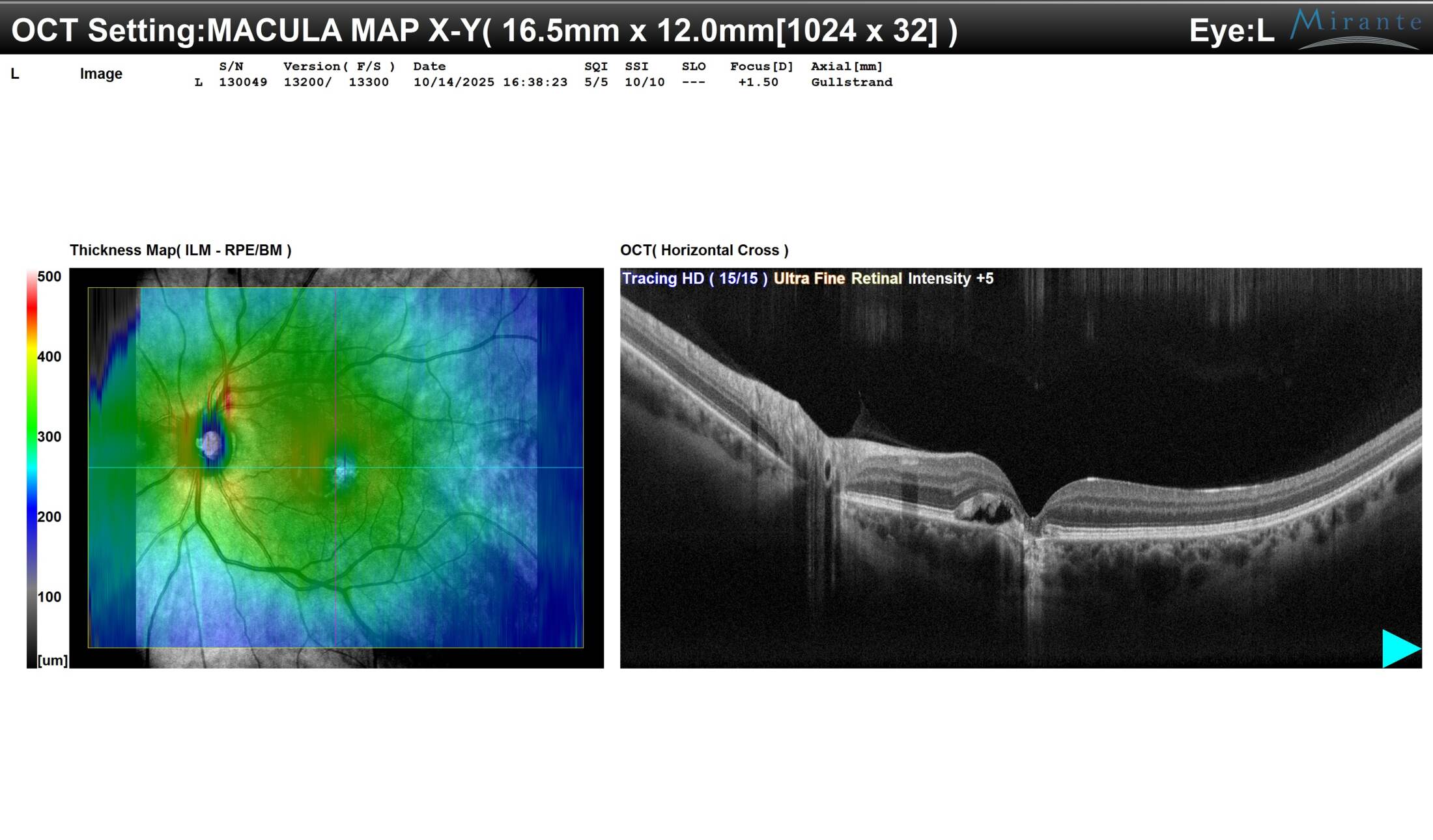
Tomografia a Coerenza Ottica – OCT (Figura 5): L’OCT dell’occhio sinistro è stato dirimente. Ha mostrato non solo il distacco sieroso del neuroepitelio, ma anche un’area di atrofia dell’epitelio pigmentato retinico e degli strati retinici esterni in sede perifoveale.
Questa perdita di tessuto nervoso è la causa diretta del calo visivo e dello scotoma percepito dal paziente.
Figura 5: OCT maculare dell’occhio sinistro (OCTOS.bmp). Oltre al distacco sieroso, si nota un assottigliamento e una disorganizzazione degli strati retinici esterni (area atrofica), che giustifica il visus di 4/10.
Autofluorescenza (Figura 6): L’immagine ha confermato la presenza di un’area di ipo-autofluorescenza (scura) mista a iper-autofluorescenza, un pattern che corrisponde alla presenza di atrofia (cellule dell’EPR morte, che non emettono fluorescenza) accanto ad aree di sofferenza cellulare.
Figura 6: Autofluorescenza dell’occhio sinistro (AUTOFOS.bmp). Il pattern misto con un’area centrale scura (ipo-autofluorescente) conferma la presenza di atrofia dell’EPR.
Discussione e Conclusioni
Questo caso clinico è un eccellente esempio di come la malattia di Best possa evolvere in modo asimmetrico. L’occhio destro, pur avendo un evidente distacco sieroso, mantiene una funzione visiva perfetta grazie all’integrità dei fotorecettori. Al contrario, l’occhio sinistro dimostra come la progressione della malattia verso la fase atrofica porti a un danno funzionale irreversibile.
I punti chiave da portare a casa sono:
1. La struttura non è sempre uguale alla funzione: L’OCT dell’occhio destro mostra un’alterazione anatomica significativa, ma il visus è di 10/10. Questo sottolinea l’importanza di non basarsi solo su un esame, ma di integrare sempre i dati strumentali
con la clinica.
2. L’importanza dell’imaging multimodale: L’uso combinato di retinografia, OCT e autofluorescenza è stato fondamentale per comprendere appieno i diversi stadi della malattia nei due occhi e per correlare le alterazioni strutturali con i deficit funzionali.
3. Prognosi e Follow-up: Il paziente dovrà essere monitorato nel tempo. L’occhio destro, attualmente nello stadio vitelliforme, potrebbe evolvere verso stadi più avanzati, come quello già presente nell’occhio sinistro. Il follow-up periodico con OCT e autofluorescenza sarà cruciale per intercettare precocemente eventuali cambiamenti.
La gestione della malattia di Best è principalmente basata sull’osservazione e sul trattamento di eventuali complicanze, come la neovascolarizzazione coroideale. Questo caso dimostra l’importanza di una diagnosi accurata e di un attento monitoraggio per fornire al paziente una prognosi corretta e gestire le sue aspettative.
OCT OD
OCT OS
RETINOGRAFIA OD
RETINOGRAFIA OS
AUTOFLUORESCENZA OD
AUTOFLUORESCENZA OS